紫外線照射による水中病原微生物の不活化
Inactivation of water pathogenic
microorganisms by Ultraviolet irradiation
1.水の消毒処理について
人が生活する上で安全な水の供給が確保されていることは必須の条件である。特に都市生活を送るためには上水道システムが安全に管理されている必要がある。ここでいう安全な水という定義は人の健康に害を与える確率(リスク)が社会通念的に無視できるほど小さいという意味である。とはいえ近年、市販のペットボトル水の普及などにより、水道水をそのまま飲料に使うということが一般的でなくなってきている。しかし生活する上で水道水に接触するのは何も直接飲料する場合には限らない。入浴やシャワーなどの際に、水が体内に入ってくる可能性は容易に想像できるであろう。
このように人の健康に直接関係している水供給システムの中で、今大きなパラドックスが生じていることをご存じだろうか。水道水を飲むと実感される方もおられるだろうが、水道水には必ず塩素が入っている。日本では浄水処理において塩素注入を行うことが法律で決まっており、水道末端において残留塩素濃度で0.1
mg/L以上を確保しなければならないことになっている。
塩素処理は水道水中の病原微生物による病気の伝染を防ぐ消毒が主な目的である。近代水道は元々伝染病予防の面から普及したことを考えると、消毒は欠くべからざる処理プロセスであるといえる。ところがこの塩素消毒処理によって発ガン性物質が生じてしまうことが1970年代後半から問題にされてきた。水中に溶存している有機物と投入された塩素が反応してトリハロメタン(クロロホルム、ブロモジクロロメタン、ジブロモクロロメタン、ブロモホルム)などの発ガン性物質が塩素消毒副生成物として生成してしまうのである。
この事実によって水道界がうけた衝撃は大きく、それまでの「塩素を入れておけば健康に関しては大丈夫」といった考え方を根本から見直さなければならなくなったのである。また法律の面からも平成4年に環境基準をはじめとする水質基準の大幅な改正が行われ、健康に関する基準項目として消毒副生成物を含む17項目が付け加えられた。
当然のことながら、投入塩素量を減らせば消毒副生成物の生成量を減らすことができるので、塩素注入量を減らすなどで対処している。しかし塩素注入量を減らせば病原微生物のリスクは当然上昇するわけで、そのリスクを安全域に抑えながら、発ガン性物質のリスクを抑えなければならないという、従来より困難なプロセス管理を強いられることになったのである。
そこでにわかにクローズアップされてきたのが、塩素に代わる消毒処理法である。特に紫外線殺菌処理は、装置が相対的に単純であり維持管理が容易なこと、薬品投入を行わないので残留物質が存在しないこと、副生成物が生成しにくいこと等の長所をもち、現在でも食品工業、電子工業などの産業用の用水処理に広く使われている。
表-1 各国における殺菌手法
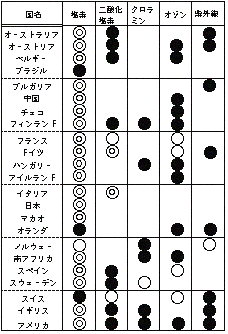
◎:主たる手法
○:よく使用されている手法
●:場合により使用される手法
日本では上述したように上水道においては塩素注入が法的に義務づけられているため、浄水場における適用例はないが、下水処理場における消毒処理については適用例が報告されている。世界に目を向けてみれば、表−1に示したようにオランダ、イギリス、ノルウェ−などヨーロッパにおいて実用例が見受けられる。特にオランダは塩素代替処理においては最も先鋭的であり、将来はできるだけ塩素を使用しない消毒方法に切り替えていくとしており、紫外線の導入を進めていくとしている。この様な流れは日本においても将来求められるようになると考えられる。
2.紫外線消毒処理の原理
そもそも紫外線消毒とはいかなる原理で行われるものなのだろうか。太陽光には殺菌作用があることは経験的に昔から知られているが、これが短波長の紫外線の作用によることが明らかにされたのは19世紀の終わりのことである。一般的に紫外線とは電磁波(光)の一種で、100-380nmの波長に含まれる(図1)。
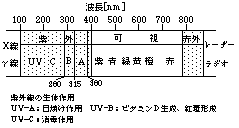
図1 紫外線の波長領域
さらに紫外線は太陽光に含まれる近紫外(300-380nm)と、含まれない遠視外(190-300nm)、そして真空中でしか測定できない真空紫外(100-190nm)に分けられる。このうちで遠紫外光は生物の遺伝子に損傷を誘発する効果が高くUV-Cとも呼ばれる。屋外において日焼けの原因になる紫外線は主に320nm以上の光でありUV-Aと呼ばれる。この光は遠紫外光に比べて消毒効率はかなり低くなる。190nm以下の波長では空気中の酸素によって吸収されオゾンを生成することが知られている。
現在、一般に使用されている紫外線ランプとは水銀蒸気を低圧(6μHg)で石英管に封入したもので、254
nmの波長を特異的に発生するランプである。石英管を用いるのは、通常のガラスでは300nm以下の波長光を吸収してしまい、遠紫外光が透過できないからである。
生物の細胞内の核酸すなわちDNAとRNAは5種類の塩基(アデニン−A、シトシン−C、グアニン−G、チミン−T、ウラシル−U)から構成されているが、これらは紫外域において図2の様な光吸収スペクトルをもつ。
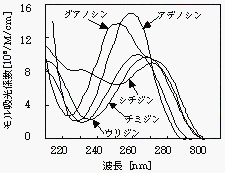
図2ヌクレオシドの紫外域吸収スペクトル
一般に炭素同士の単結合は230nmより長い波長側では吸収を持たないから、紫外線による核酸の化学的変化は、核酸に含まれる二重結合への光子吸収が原因と考えられる。ランプより照射された波長254nmを主体とする紫外光はDNA及びRNAの塩基に吸収される。吸収された光量子エネルギーにより、チミン−チミン、チミン−シトシン、シトシン−シトシン、ウラシル−ウラシル等の二量体(T^T、T^C、C^C、U^U)が形成される。このような二量体が形成してしまうと、細胞分裂の際の複製の際、そこで複製が止まってしまう(つまり自分のコピーを作れない=増殖できない)。これをDNA、RNAの不活化と呼ぶ。つまり紫外線消毒というのは微生物を殺すのではなく、微生物を増殖できなくさせるという原理に基づいているのである。そのため殺菌という言葉は適当でなく、厳密には消毒や不活化という表現方法を使う。
3.不活化速度論(標的論)
DNAやRNAが紫外線照射によって損傷を受け、微生物が不活化していく速度はどの様に考えれば良いのだろうか?よくモデルとして考えられるのが標的論という抽象化した概念である。これは目的の細胞(例えば大腸菌)の中に紫外線で損傷を受けやすい部位があるとする。これを"標的"
(target)と名付ける。標的が損傷した場合これを"ヒット"
(hit)とよぶ。
細胞に紫外線照射を作用させたとき、細胞内の標的に平均λ個のヒットが生じるとする。ヒットはall or
nothing型で中間の型は存在せず、しかも互いに独立に生成されλの値は小さいとすれば、反応の現れ方の予言は、簡単な確率論の問題である。すなわちある特定の標的内に実際x個のヒットが生じている確率p(x)はポアソン分布で表される(式(1))
p(x)=exp(-λ)・λx/x! (x=0,1,2・・・)(1)
細胞の生残率Sがヒット数λのどの様な関数になるかは、細胞内の標的の数と標的の性質を仮定しなければならない。
3.1 1ヒット性1標的
標的が細胞内に1個しかない(すなわちその標的の1ヒットで細胞が死ぬ)場合は、生残率Sはヒットを受けない確率p(0)に等しくなるので、式(1)より次の式になる。
S = exp(-λ) (2)
λは紫外線線量に比例する。従って
λ = k・I・t (3)
k:比例定数、I:紫外線線量率、t:照射時間
(2)、(3)式から次式を得る。
S =
exp(-k・I・t) (4)
すなわち生残率は一次反応的に減少することがわかる。
3.2 1ヒット性多重標的
細胞内に標的がm個あると仮定する。またそれぞれの標的は1ヒットで不活化されるとする。このとき細胞内の標的のm個全てが不活性化されたとき細胞が不活化されるとする。ある標的がヒットされている確率は、(2)式より(1-
exp(-λ))となる。従ってm個の標的が全て死んでいる場合は、(1- exp(-λ))mであるので、生残率は次式となる
S = 1 - (1- exp(-λ))m = 1 - (1-
exp(-k・I・t))m (5)
この場合、縦軸に生残率の対数、横軸に時間をとってプロットすると、上方で肩があり下方に行くに従って、直線となる関係が得られる(shoulder
curve)。
3.3 実際の不活化実験の結果
主な病原微生物には原虫類、病原細菌、病原ウイルスがある。それぞれ標的論から見れば、比較的長いDNAをもち複雑な構造をもつ原虫類や細菌については1ヒット性多重標的モデルが良く当てはまり、一方、単純な構造をもつウイルスは1ヒット性1標的のモデルが良く当てはまる。
図3、図4はそれぞれの微生物の紫外線不活化実験の結果例を示したものである。
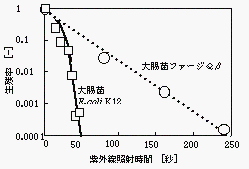
図3 ファージと大腸菌の紫外線不活化
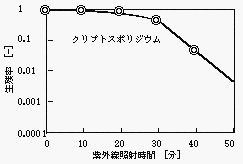
図4 クリプトスポリジウムの紫外線不活化
ここで示した大腸菌ファージQβとは、大腸菌に寄生するウイルスであり、その構造が人由来の水系感染性病原ウイルスであるピコルナウイルスに非常に似ていることからモデルウイルスとしてよく使用されているものである。大腸菌は単離株(E.coli
K12
F+(A/λ)を用いた。クリプトスポリジウムは畜産排水がその汚染源と考えられいる病原性原虫であり、人に感染して下痢を引き起こす。平成7年度に埼玉県で水系感染事故による集団感染が発生し、にわかに注目されているものである。このクリプトスポリジウムについては塩素耐性が細菌の数千倍と高く、いまだに効果的な消毒技術が見つかっていないやっかいな代物である。
図3からわかるようにウイルスは一次反応的に減少しており、構造が相対的に複雑な大腸菌、クリプトスポリジウムは両者とも肩のある曲線となり、1ヒット多重標的モデルが当てはまることがわかる。この実験結果から大腸菌E.coli
K12
F+(A/λ)とクリプトスポリジウムは、推定致死ヒット数でそれぞれ約900、約100と推定される。
これらの実験結果からウイルス類は相対的に単純な構造であり、不活化速度の解析も容易であることから微生物を用いた紫外線線量計としての応用が考えられる。特にファージを用いる場合は、その測定方法が容易であるというメリットがある。
紫外光の光量測定には従来から光量測定用メータや化学物質の光化学反応量を用いた化学線量計が使用されているが、いずれも遺伝子吸収波長の特性を表現するものではない。一方、ウイルスまたはファージの不活化速度から紫外線線量を算定する方法は、換言すればDNAまたはRNA損傷速度から紫外線を算定するものであり、ウイルスも他の微生物もその不活化機構が同じであることを考慮すると、消毒効果を評価するのに最適の方法と思われる。
またこの方法は装置の形状を考慮することなく、全体の消毒処理性能を簡易に測定できる方法であり、その応用範囲は非常に大きいものと期待されている。
4.紫外線処理後の光回復現象
4.1 光回復とは
紫外線照射は遺伝子を損傷することによって病原微生物等を不活化し水中病原微生物リスクを減らす事ができるのだが、自然のからくりは侮れないもので、生物にはその損傷遺伝子を自己修復する機能が備わっているものが多い。考えてみれば、原始生物が存在していた世界は太陽光からの遠紫外線が大量に降り注いでいた世界であり、遠紫外線によって損傷を受ける頻度は現在とは比べものにならない程であっただろう。その中で生物が紫外線による損傷を修復する機能を備えていったのは、当然の成り行きであり、現在でもその機能が受け継がれていると考えれば納得せざるを得ない。
修復機能の中で主なものに、光回復がある。これは細胞内に存在する光回復酵素が近紫外光を用いて活性化し、紫外線によって生じた二量体を元の塩基に開裂させてしまうものである(図5参照)。
なおこの機構は比較的単純な構造であるウイルスには備わっておらず、大腸菌などの細菌類より高等な微生物に備わっているものである。一説によればヒトもこの酵素を持っているということである。これを酵素的光回復と呼ぶが、遠紫外光によって損傷を受けた細胞が近紫外光によって修復するといった機構は驚愕に値する。
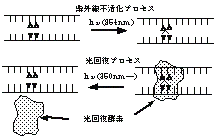
図5 光回復のメカニズム
しかし感心ばかりはしていられない。病原微生物の中には光回復をすると考えられているものが数多く存在する。従って紫外線処理によって病原微生物リスク管理を行う上では、光回復がどの様な因子の影響を受け、どの位の速度で回復するのかを把握しておく必要がある。
4.2 光回復モデル
紫外線照射によって不活化された細菌の光回復速度についてはDulbecco(1955)によって次のような一次反応式が提唱されている。
dS/dt = r・(Sm -
S) (6)
r:光回復速度定数、Sm:最大光回復生残率
上式でのSmは紫外線照射を行う前の生残率(すなわち1)より小さい値になる。従って、光回復を十分させた後でも紫外線照射を行う前の状態に完全に戻るわけではなく、回復しない菌も存在することになる。このSmと紫外線照射直後(光回復前)の生残率Soの関係は既存の研究により次の関係があることがわかっている。
Sm/So(am/ao) (7)
am:最大光回復生残率に関する不活化定数
ao:紫外線照射直後生残率に関する不活化定数
下水処理場流入水から単離したE.coliを用いて行った実験結果を図6に示す。
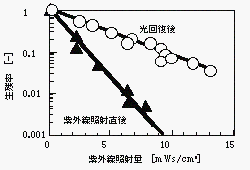
図6 単離E.coliの紫外線不活化と光回復
この図において上式(7)の関係が示されていることがわかる。つまり、紫外線を多く照射すればするほど光回復出来なくなる菌数が増加することがわかった。従って細菌の不活化に必要な紫外線照射量を求める場合は光回復を考慮する場合は不活化速度定数amを、光回復を考慮しない場合はaoを用いれば良いことがわかる。しかし、別の報告によれば紫外線照射後に数時間暗所に保存しておけば、最大光回復量が減少するという結果も示されており、光回復に関は研究して行かねばならない、まだまだ未知の機構が存在するようである。
4.3 光回復速度とその影響因子について
光回復速度に影響を与える因子として、まず光量を考える。第一に不活化する際の紫外線照射量は光回復速度に影響を与えるのだろうか。
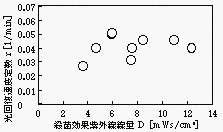
図7 光回復速度定数と紫外線照射線量の関係
図7は光回復速度定数rと照射紫外線量I・tの関係を示している。照射紫外線線量は光回復速度には影響しないようである。
次に光回復させる際の近紫外光について考える。図8は近紫外光線量率Uと回復速度定数rの関係を示している。これはおおよそ比例関係が得られた。
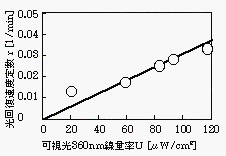
図8 光回復速度と近紫外光量の関係
光回復速度は、二量体と活性化した光回復酵素との反応で起こると考えられる。また活性化光回復酵素量は近紫外線量に比例すると考えられる。
E = a・U
(8)
E:活性化光回復酵素量、U:近紫外光量
a:活性化光回復酵素生産比例定数
さらに光回復速度は、回復できるが未だ回復していない細菌の生残率差(Sm
- S)と活性化光回復酵素量Eに比例すると仮定すれば、次式が得られる。
dS/dt = b・E・(Sm - S) = b・a・U・(Sm - S)
(9)
b:光回復酵素速度定数
(9)式を前述の(6)式と比較すればr=
a・b・Uとなり、光回復速度定数は近紫外光量に比例することが示される。
以上の結果から光回復速度は消毒の際の紫外線光量には依存せず、光回復時の近紫外光量に比例することがわかった。
5.最後に
以上、紫外線照射という比較的単純な消毒処理法について述べてきた。しかし、その対象が微生物となると、その現象を説明するための作用メカニズムは非常に複雑であり未知の部分が多く、研究対象としても奥が深いものであることがわかっていただけると思う。ここで紹介したのはそのほんの一部に過ぎないし、いろいろな研究の切り口が残されていると思われる。例えば、近年の遺伝子学的手法の発展などにより、その手法を用いてのメカニズム解明など期待の膨らむところである。
また、装置の方に目を向けてみると、ここで述べてきた定圧水銀ランプの他にも近年いろいろな消毒用ランプが開発されてきている。例えば、封入する水銀圧力を数百mmHgにした中圧紫外線ランプがある。これは一本の照射エネルギーが高く大容量の消毒に向く装置であると期待されている。ただし、照射波長スペクトルが254nmだけでなく200nm〜400nmと広い波長域にわたっているため、この波長光が消毒効果にどの様にかかわってくるかも研究課題である。また瞬間的に高いエネルギーを不連続的に照射するパルスUVランプも実用化が検討されている装置である。基本的にはここで述べてきた遠紫外光の消毒機構が主な作用機序であると考えられるが、瞬時に通常の100〜1000の強さの光が照射される場合の、微生物への影響というのもこれまでとは違った機構が働くかもしれず、興味深いテーマである。
6.参考文献
1.
Dulbecco, R.,"Photoreactivation", Radiation Biology, Vol.2, pp.455-486, McGrow
Hill Book Co. Inc., New York, 1955.
2. 近藤宗平:分子放射線生物学、学会出版センター、1984.
3.
大垣眞一郎:紫外線照射による消毒技術の基礎概念、造水技術、Vol.15、No.1、pp.33-39、1989.
4. Kamiko, N. et
al.,"RNA Coliphage Qァ as a bioindicator of the Ultraviolet Disinfection
Efficiency", Wat. Sci. Tech., Vol.21, No.3,
pp.227-231,1989.
5.加藤益雄:紫外線消毒技術の適用分野、造水技術、Vol.15、No.1、pp.33-39、1989.
6.
L.O.Hiisvirta, "Disinfection and Disinfection byproducts",proc. of IWSA 1993
congress, 1993.
7.National Water Research Institute (USA), "UV Disinfection
Guidelines for Wast water Reclamation in California and UV Disinfection Research
Needs Identification",1993
8. 石山栄一:清涼飲料水製造における紫外線殺菌の利用、食品機械装置、Vol.30, No.8,
pp.71-81,
1993.
9.鹿島田浩二:紫外線消毒における光回復、用水と廃水、Vol.38、No.5、pp.359-364、1996.
10.
大瀧雅寛他:紫外線照射および紫外線−光触媒処理における細菌の光回復、環境工学研究論文集、Vol.34、pp.75-82、1997.
>> Back <<








